Il carlumab è un anticorpo monoclonale umano ricombinante, appartenente alla superfamiglia delle IgG, che interagisce con il ligando della citochina 2 (CCL2), detta anche proteina chemoattrattiva dei monociti. L'uso dell'anticorpo è stato studiato in campo oncologico e immunologico, esplorandone le potenzialità terapeutiche nei confronti dello scleroderma sistemico, dell'aterosclerosi, della nefropatia diabetica, della cirrosi epatica e del diabete mellito di tipo 2. Prodotto dalla Janssen Pharmaceutica fino al 2012, il suo sviluppo in laboratorio è stato in seguito sospeso a causa della limitata efficacia dimostrata dall'anticorpo in alcune sperimentazioni cliniche.
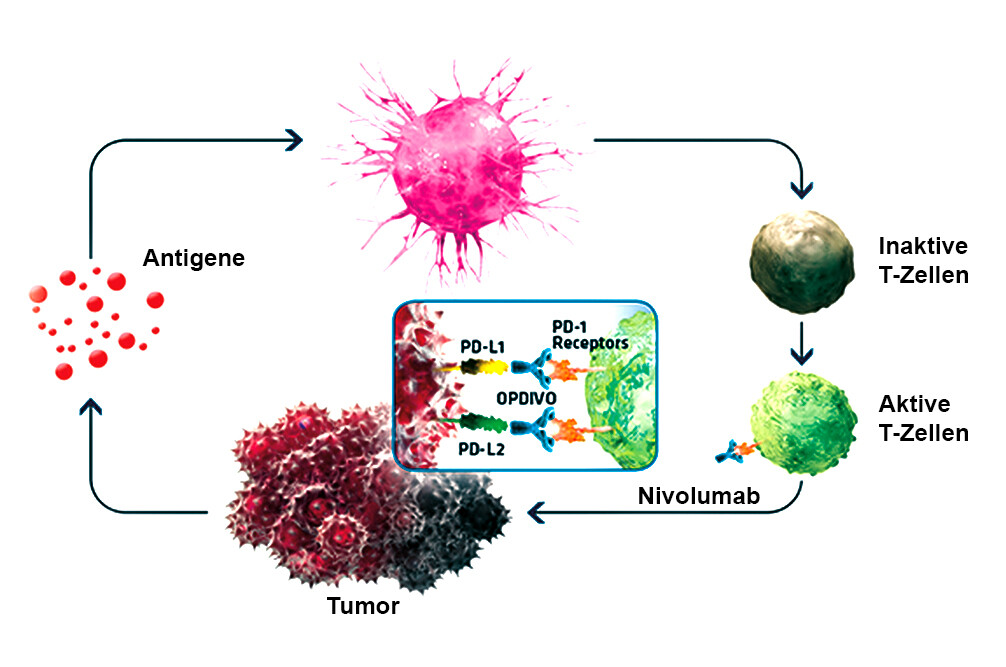
Si suppone che il legame del carlumab con il ligando della citochina 2 abbia un effetto inibitorio sull'angiogenesi, riducendo pertanto la proliferazione neoplastica. Alcuni studi clinici focalizzati sull'uso del carlumab sono stati effettuati sia in colture cellulari in vitro che su esseri umani e su esemplari vivi di topo, allo scopo di studiare l'efficacia, la sicurezza e la posologia dell'anticorpo; alcuni di questi studi hanno raggiunto la fase I, altri la fase II. Ulteriori studi clinici con il carlumab hanno riguardato pazienti affetti da fibrosi polmonare idiopatica, da carcinoma della prostata metastatico resistente all'asportazione degli organi genitali e da altre neoplasie, sia epiteliali che mesenchimali.
Note